- Matériel et outils
Désodoriser le frigo, se laver les dents, favoriser la digestion, laver les surface salles... Et surtout, c'est le chouchou des expériences de wikidébrouillard !
Il est parfois appelé bicarbonate de soude mais il ne faut surtout pas le confondre avec la soude qui est très corrosive et peut être très dangereuse.
Étape 2 - Manipulation
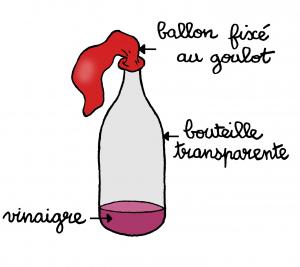
- Verser du vinaigre dans la bouteille (jusqu'à environ 4 ou 5 cm de haut).
- Verser 2 cuillères à soupe de bicarbonate de sodium à l'intérieur du ballon de baudruche, à l'aide de l'entonnoir.
- Enfiler l'ouverture ballon sur le goulot de la bouteille. S'assurer que le ballon tient bien.
- Soulever le ballon pour faire tomber le bicarbonate dans la bouteille.
Comment ça marche ?
Observations : que voit-on ?
Le contenu de la bouteille mousse, le ballon se gonfle et reste gonflé sur la bouteille.
Mise en garde : qu'est-ce qui pourrait faire rater l'expérience ?
Les quantités de bicarbonate et de vinaigre peuvent jouer sur le gonflement du ballon : plus il y a de bica et vinaigre, plus il y a de gaz qui se créé, plus le ballon gonfle !
Bien tenir le ballon pour ne pas que le gaz s'échappe du goulot
Explications
De manière simple
Lorsque le bicarbonate tombe dans la bouteille, des bulles se forment dans le liquide et le ballon se met à gonfler. Ces bulles sont produites par la réaction chimique entre le vinaigre et le bicarbonate. Cela nous permet de dire qu'un des produits de la réaction chimique entre le vinaigre et le bicarbonate est un gaz, puisqu'il gonfle le ballon.
Grâce au ballon, on capture un gaz invisible produit par une réaction chimique !
Le vinaigre est un liquide, le bicarbonate est une poudre composée de minuscules grains solides. Lorsque ces deux produits réagissent ensemble (on les appelle des réactifs), ils donnent naissance à un nouveau produit qui lui est un gaz. Ce dernier n'est pas le seul produit issu de la réaction. En effet, lorsqu'on goûte le liquide, il ne pique plus la langue comme le vinaigre mais il a un goût salé !
Le vinaigre et le bicarbonate se sont aussi transformés en une sorte de sel qui est dissous dans le liquide. Ce sel et le gaz sont les produits de la réaction.
Plus d'explications
Nous avons affaire à une réaction acido-basique. Ici le vinaigre, qui contient de l'acide éthanoïque, joue le rôle de l'acide et le bicarbonate de soude, aussi appelé hydrogénocarbonate de sodium, celui de la base.
En solution, ce dernier se dissout en formant deux ions différents : les ions sodium et hydrogénocarbonate.
NaHCO3 --> Na+ + HCO3-
Ce sont ces derniers qui vont réagir avec le vinaigre pour former de l'eau et du dioxyde de carbone selon la réaction suivante :
CH3COOH = CH3COO- + H+
HCO3- + H+ = CO2 + H2O
______________________________________________________________________
CH3COOH + HCO3- --> CH3COO- + CO2 + H2O
On obtient alors une eau au goût salé en raison de la présence en début de réaction des ions sodium. En effet, lorsque l'on dissout du sel (chlorure de sodium) dans de l'eau, on obtient bien ces ions sodium responsables du goût salé (et des ions chlorure).
Le dioxyde de carbone, quant à lui, ne peut pas se dissoudre dans l'eau. Il remonte donc à la surface du liquide sous forme de bulles, avec la poussée d'Archimède.
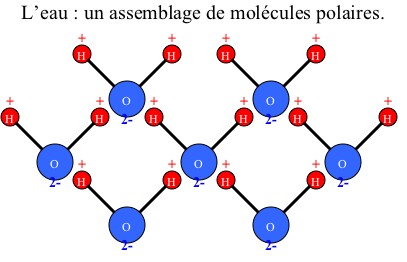
En effet, ce gaz est non polaire tout comme peut l'être l'huile. En revanche, l'eau est une molécule polaire : sa configuration provoque l'apparition de "pôles" négatifs et positifs (voir schéma un peu plus bas).
On peut facilement se rendre compte que les molécules non polaires et polaires s'associent en général très difficilement (exemple : eau + huile = eau + huile). Pour expliquer cela, il faut observer ces molécules d'un peu plus près...
Pour commencer prenons l'eau (H2O) sous forme liquide :
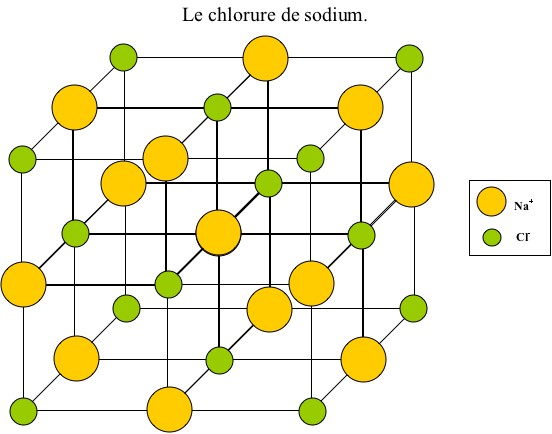
Puis du sel (NaCl) :
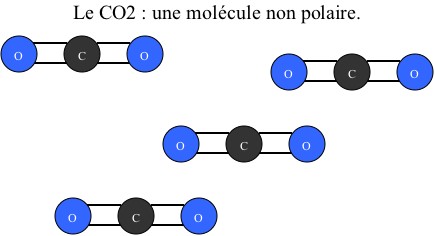
Puis du dioxyde de carbone (C02) :
Remarque : La polarité de ces molécules est due à leur forme. Lorsque tous les atomes sont alignés, il n’existe pas de moment dipolaire entre eux. Au contraire, lorsqu’ils sont configurés différemment, les différentes charges ne sont plus alignées et il y a création d’un moment dipolaire et donc de « pôles ».
Et faisons des "mélanges" :
Dans un premier temps, on mélange l'eau avec le sel. Les molécules d'eau s'associent aux molécules de sel par "pôles" préférentiels (+ avec - et - avec +). Elles entourent ces molécules pour former une sorte de barrière où seules les molécules d'eau peuvent s'attacher. La forme cristalline du sel disparaît alors pour former les ions Na+ et Cl-. On parle de l'hydratation du sel.
Dans un second temps, on mélange le CO2 avec un liquide acide. Les molécules d'eau ne peuvent s'associer aux molécules de dioxyde de carbone car ces dernières ne possèdent pas de "pôles". Elles ne peuvent donc pas hydrater le dioxyde carbone et celui-ci reste sous forme de gaz.
Éléments pédagogiques
Objectifs pédagogiques
Comprendre la création d'un gaz, les réactions chimiques entre deux éléments, la polarité des molécules.
Dernière modification 19/08/2020 par user:Nathanaël Latour.
Draft